Pokrok vo výskume aplikácie materiálov z titánových zliatin v ortopédii
Zliatina titánusa stal bežne používaným materiálom v ortopedickej klinickej praxi (ako sú oceľové dlahy na vnútornú fixáciu a umelé kĺby) vďaka svojim vynikajúcim mechanickým vlastnostiam a osteogénnym schopnostiam, ale má obmedzenia, ako je inertnosť kovu a uvoľňovanie iónov. Nová zliatina titánu optimalizuje fyzikálno-chemické a biologické vlastnosti prostredníctvom materiálovej vedy. Tento článok hodnotí pokrok vo výskume ortopedickej aplikácie a poskytuje referenciu pre vývoj v tejto oblasti.
Materiály ortopedických implantátov sú najmä kovy vrátane nehrdzavejúcej ocele, kobaltu a jeho zliatin, titánu a jeho zliatin atď. Z nich zliatiny titánu sú široko používané v klinickej praxi vďaka svojim vynikajúcim výhodám, ako je biokompatibilita, vysoká pevnosť, odolnosť proti korózii a nízka hustota. V posledných rokoch mnohí vedci vykonali-hĺbkový výskum v oblasti metód spracovania a výroby, modifikácie povrchu, veľkosti pórov a pórovitosti titánových zliatin s cieľom vyriešiť problémy s vysokým modulom pružnosti, povrchovou inertnosťou a uvoľňovaním kovových iónov, ktorým čelia zliatiny titánu v klinických aplikáciách. Tieto štúdie pomôžu nielen zlepšiť biologický aplikačný účinok titánových zliatin, ale tiež zlepšia osseointegračné vlastnosti, antibakteriálne vlastnosti a bezpečnostné vlastnosti in vivo. V tomto článku sú stručne zhrnuté povrchové modifikácie a modifikácie, štrukturálne vlastnosti a rôzne typy titánových zliatin titánových zliatin s cieľom získať-hĺbkové pochopenie súčasného stavu, výhod a nevýhod titánových zliatin v biologických aplikáciách, ako aj ich výskumu a smerovania budúceho vývoja.
1. Štruktúra kosti a výhody a nevýhody zliatiny titánu
Kosť má vrstvenú štruktúru na makroskopickej, mikroskopickej a nanoúrovni a obsahuje organické aj anorganické minerály. Podľa štruktúry a hustoty ju možno rozdeliť na trabekulárnu kosť a kortikálnu kosť. Trabekulárna kosť sa skladá z poréznej siete s pórovitosťou 50 % ~ 90 % a modulom pružnosti 0,02 ~ 2 GPa, zatiaľ čo kortikálna kosť je pevná, s pórovitosťou 3 % ~ 5 % a modulom pružnosti 3 ~ 30 GPa. Kosť sa neustále mení v dôsledku rôznych aplikovaných tlakov, takže akýkoľvek nesúlad modulu medzi implantátom a kosťou môže viesť k resorpcii kosti spojenej s Wolffovým zákonom. Ideálny ortopedický implantát by mal podporovať regeneráciu kosti v poškodenej oblasti a zároveň obnoviť fyzickú funkciu kosti. Vo všeobecnosti by mali byť blízko k prirodzeným kostiam a mali by sa riadiť nasledujúcimi základnými vlastnosťami:
(1) biokompatibilita;
(2) prispôsobenie mechanických vlastností;
(3) Vysoko porézna štruktúra.
Okrem toho sú dôležité aj antibakteriálne vlastnosti.

V ortopédii sa titánové implantáty používajú v širokom spektre aplikácií, vrátane náhrad bedrových a kolenných protéz na liečbu rôznych typov artritídy, spinálnych fúznych zariadení na zabezpečenie stability degeneratívnych a nestabilných stavcov a rôznych zariadení na fixáciu zlomenín, ako sú kovové platničky, skrutky a intramedulárne klince. Keďže počet implantačných procedúr neustále narastá, pacienti čelia mnohým rizikám, ako je bakteriálna infekcia, slabá osseointegrácia a aseptický zápal. Hoci sú titánové zliatiny známe svojou vynikajúcou biokompatibilitou a odolnosťou proti korózii, nemožno ignorovať ich potenciálne nedostatky: po prvé, neošetrené implantáty z titánovej zliatiny majú biologicky inertný povrch, ktorý ovplyvňuje ich interakciu so živými organizmami; po druhé, samotná zliatina titánu nemá antibakteriálne vlastnosti; Po tretie, napriek jeho dobrej biokompatibilite, akonáhle je oxidový film na povrchu poškodený, škodlivé kovové ióny sa môžu uvoľňovať do krvného obehu, čo môže spôsobiť vážne zdravotné problémy.
2. Povrchová úprava a úprava zliatiny titánu
Slabé skoré hojenie kosti na rozhraní kostného-implantátu sa považuje za jednu z hlavných príčin pooperačného zlyhania. V posledných rokoch vývoj technológie povrchovej úpravy priniesol nové nápady na riešenie vyššie uvedených problémov. Výskumníci pridávajú na povrch titánových zliatin určité látky, aby dosiahli anti-infekčné, osteogénne,-odolné proti opotrebovaniu, korózii-a anti-oxidačné účinky. Techniky chemickej povrchovej úpravy zahŕňajú eloxovanie, mikro-oblúkovú oxidáciu, elektroforetické nanášanie, chemické naparovanie, alkalické zahrievanie a nanášanie atómovej vrstvy.
Vytváraním chemických väzieb sa viažu nové látky so silnými väzbovými silami. Navyše pre tvarovo zložité implantáty bola prispôsobená technológia chemickej povrchovej úpravy, ktorá má veľké uplatnenie pri úprave 3D tlačových zliatin titánu. Na rozdiel od chemických metód technológia fyzikálnej povrchovej úpravy nemení chemické vlastnosti materiálov, ale pri úprave vzhľadu povrchu a mikroskopickej morfológie titánových zliatin sa spolieha na laser, vysokoenergetické častice, ultrazvuk a ďalšie technológie.
Tradičné techniky pieskovania zvyšujú drsnosť povrchu titánových zliatin, čím zlepšujú skorú stabilitu implantátov. Laser je relatívne nová technológia, ktorá mení štruktúru materiálov na úrovni nanometrov a mikrometrov. Brane⁃mark a kol. použili laserovú technológiu na povrchovú úpravu implantátu na konkrétnom mieste a potom ho umiestnili do holennej kosti a stehennej kosti a výsledky ukázali, že táto technika zlepšila ukotvenie kostného-rozhrania implantátu. Gittens a kol. vyvinuli metódu povrchovej modifikácie na vytvorenie vlastností nanometrov na titánových platniach, čo vedie k zvýšenej diferenciácii osteoblastov. Porézna titánová štruktúra bola potiahnutá viacvrstvovou želatínou a chitosanom obsahujúcim kostný morfogenetický proteín alebo vankomycín, ktorý vykazoval silnú antimikrobiálnu aktivitu proti planktónovým a adherentným baktériám.

Spomedzi rôznych povrchových náterov je najrozšírenejší plazmový nástrek hydroxyapatitu (HA) vďaka svojim výhodám, ako je jednoduchosť obsluhy a nízka cena. Okrem toho mikro-oblúková oxidácia, hydrotermálna úprava, elektroforetické nanášanie a ďalšie technológie môžu úspešne vytvárať HA povlaky na poréznych titánových povrchoch. Štúdie porovnávali plazmou nastriekané HA povlaky s elektrochemicky nanesenými HA povlakmi a výsledky ukazujú, že druhý má vyššiu drsnosť povrchu a zmáčavosť.
Biokompatibilitu možno zlepšiť potiahnutím keramiky a iných oxidov alkalických kovov. Urbanski a kol. [18] potiahli Ti6Al4V oxidom titaničitým a oxidom kremičitým a umiestnili ho do stehennej kosti potkanov a zistili, že zápalová reakcia materiálu bola mierna. Novou metódou je poťahovanie titánových zliatin poľnohospodárskym odpadom, ako je popol z ryžových šupiek, popol z listov cukrovej trstiny, arašidy a kukuričné šupky, pretože tieto materiály obsahujú veľké množstvo oxidov oxidu kremičitého a iných súvisiacich nanočastíc alebo mikročastíc. Táto metóda bola použitá v bioskle a keramike, kde sa namiesto oxidu kremičitého používajú ryžové šupky ako povlak na biosklo.
3. Štrukturálne charakteristiky zliatiny titánu
Drsný povrch materiálu priťahuje k priľnutiu viac zápalových buniek, ako sú makrofágy, čo je známe ako fenomén „drsnosti“. Zistilo sa, že priemerná drsnosť materiálu bola 0, 51 ~ 1, 36 μm, čo by mohlo podporiť polarizáciu adherentných makrofágov do fenotypu M2. Olivares-Navarrete a kol. zistili, že Ti6Al4V na drsnom povrchu zlepšil lokálne zápalové prostredie v porovnaní s Ti6Al4V s hladkým povrchom a bunky rastúce na jeho povrchu znížili hladiny pro{11}}zápalových interleukínov. Preto zliatiny titánu so špecifickou drsnosťou povrchu nielen prispievajú k regulácii skorého zápalu makrofágmi, ale aj k osseointegrácii v neskoršom štádiu.
Okrem drsnosti súvisia s rastom kostí aj ďalšie fyzikálne vlastnosti povrchov titánových zliatin, ako je zmáčavosť, zeta potenciál a povrchová energia. Okrem toho, povlak fosforečnanu vápenatého dopovaný na 3D tlačenom poréznom titáne zlepšuje skorú osseointegráciu a skracuje čas hojenia. Výskumný tím vyvinul modifikáciu pasivácie chemického činidla, ktorá selektívne podporuje adsorpciu proteínov a tým zvyšuje adhéziu osteoblastov na titánovom povrchu, čo nezahŕňa vytvorenie bioaktívnej vrstvy, ale mení povrchové podmienky, aby sa uľahčila biofixácia a skrátil sa čas rastu kosti okolo titánových implantátov.
Fyzikálne a chemické vlastnosti a morfológia materiálu priamo ovplyvňujú zmáčavosť, ktorá následne reguluje adsorpciu biomolekúl a prichytenie buniek. Hydrofilita povrchu znižuje adhéziu baktérií (oslabením van der Waalsových síl), čím sa znižuje riziko infekcie implantátu a podporuje sa skorá osseointegrácia. Tradičné zliatiny titánu sú náchylné na oklúziu a resorpciu kosti kvôli ich vysokému modulu pružnosti a je ťažké reprodukovať vrstvenú štruktúru kostného tkaniva. Porézny titánový materiál znižuje modul cez štruktúru pórov a zvyšuje kotviaci efekt pomocou rastu kostí. Techniky jeho prípravy (napr. spekanie, 3D tlač) dokážu presne kontrolovať veľkosť pórov a pórovitosť prepojených pórov.
Technológia 3D tlače má oproti tradičnej výrobe dvojaké výhody: mikroskopické prispôsobenie prirodzeného kostného modulu prostredníctvom vopred nastavených pórov, aby sa znížilo riziko maskovania a uvoľnenia stresu; Na makroskopickej úrovni sa CT skenovanie používa na dosiahnutie duálnej mechanickej a morfologickej adaptácie komplexných kostných defektov.
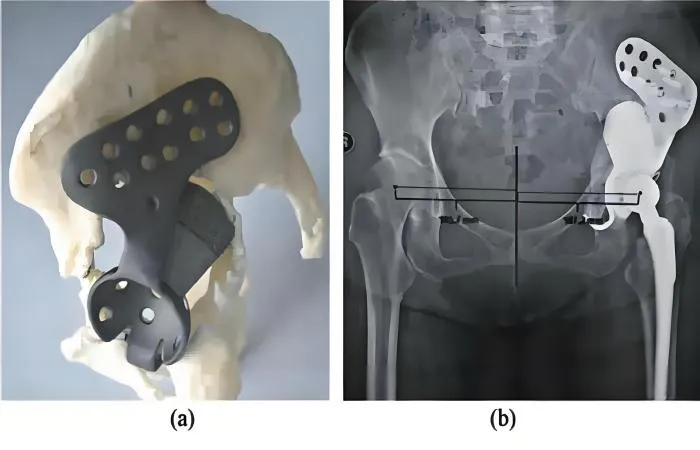
Nová spekaná porézna titánová zliatina úspešne simuluje neusporiadanú štruktúru a modul pružnosti hubovitej kosti prostredníctvom 75% pórovitosti. Experimenty in vitro ukázali, že táto štruktúra významne podporovala adhéziu a proliferáciu osteoblastov a jej osseointegračný výkon bol lepší ako u 3D tlačeného porézneho titánu. Jeho štrukturálne charakteristiky (veľkosť pórov, pórovitosť, priestorová distribúcia atď.) ovplyvňujú osseointegráciu tromi mechanizmami: (1) mechanická adaptácia vlastností; (2) Spájanie pórov na podporu migrácie kostných progenitorových buniek; (3) Optimalizujte transport živín/kyslíka a vaskulárnu infiltráciu.
Veľkosť pórov a pórovitosť sú hlavné regulačné parametre: selektívne štúdie tavenia laserom ukazujú, že veľkosť valcových pórov 632 μm je vhodnejšia pre rast kostí ako 309 μm/956 μm a veľkosť pórov 801 μm môže zlepšiť počiatočnú stabilitu. Kritický prah ukázal, že < 400 μm bránilo penetrácii buniek, > 900 μm viedlo k nedostatočnému kontaktu s kosťou a rozsah pórovitosti 75 % - 85 % bol optimálny.
Pokiaľ ide o typ zliatiny titánu, na trhu dominuje Ti6Al4V, existuje však cytotoxické riziko uvoľňovania iónov Al/V. Nové zliatiny ako Ti-15Ta-10.5Zr a Ti-13Nb-13Zr znižujú modul pri zachovaní pevnosti úpravou elementárneho zloženia. Za pozornosť stoja inovatívne smery ako superelasticita zliatin niklu a titánu a antibakteriálne vlastnosti medi/striebra Ti6Al4V.
Súčasné výzvy sa zameriavajú na: (1) presnú transformáciu zliatinovej mriežkovej štruktúry technológiou aditívnej výroby; (2) Je potrebné posilniť overovanie celého reťazca in vitro, in vivo a klinicky. Budúci výskum by sa mal zamerať na kvantitatívny vzťah medzi štrukturálnymi parametrami a biologickou aktivitou, aby sa podporil vývoj personalizovaných implantátov na opravu kostí.
4. Zhrnutie a výhľad
Zliatiny titánu sa používajú ako materiály na umiestnenie od 60. rokov minulého storočia. Odvtedy vedci skúmali zmenu zloženia zliatiny a povrchových vlastností, aby vyvinuli materiál s najlepšou kombináciou mechanických a chemických vlastností. Rôzne moderné procesy spracovania, ako aj vhodné povrchové nátery a úpravy na dosiahnutie požadovaných vlastností titánových implantátov. Na vývoj titánovej zliatiny, ktorá je húževnatá, biokompatibilná, odolná voči korózii-a opotrebeniu-, je potrebných viac zdrojov a výskumu.
Pochopením rôznych charakteristík titánových zliatin sú navrhnuté rôzne riešenia problémov vysokého modulu pružnosti a povrchovej inertnosti titánových zliatin a povrchová modifikácia a povrchová modifikácia sú bežne používané metódy na zvýšenie povrchovej aktivity titánových zliatin. Výroba poréznych titánových zliatin nielen rieši problém vysokého modulu pružnosti, ale tiež zvyšuje biologický výkon osseointegrácie. Stále však existuje veľa problémov, ktoré je potrebné prediskutovať a vyriešiť v procese výroby rôznych poréznych zliatin titánu. Aplikácia funkcionalizovaných povlakov poréznych štruktúr a objav trabekulárnych biomimetických štruktúr poskytuje lepšie možnosti pre pokrok v biologických aplikáciách titánových zliatin. V budúcnosti sa očakáva, že popri zlepšovaní mechanickej štruktúry a ďalších vlastností titánových zliatin sa bude neustále zlepšovať nanášanie biologických funkčných povlakov na povrch titánových zliatin a budú sa dosahovať nové pokroky a objavy v oblasti zvyšovania lokálneho rastu kostí, osseointegrácie, antibakteriálnych a anti-infekcií.

